Сепсис Новорожденных Ppt
- Сепсис как генерализованное инфекционное заболевание, пути заражения им новорожденных, возбудители и способствующие факторы. Клиническая картина протекания сепсиса, его классификация в зависимости от входных ворот и возбудителя, профилактика и лечение. Медицина, русский язык.
- Гр «-» сепсиса у новорожденных 32. Предрасполагающие факторы, нарушающие (снижающие).
caption id='attachment9341' align='alignleft' width='280' Сепсис новорожденных/caption Что такое сепсис новорожденных Неонатальный сепсис — это бактериальная инфекция, развивающаяся в первые 90 дней жизни. Проявления его разнообразны и включают снижение спонтанной активности, энергичности сосания, апноэ, брадикардию, нестабильность температуры, дыхательную недостаточность, рвоту, диарею, увеличение живота, беспокойство, судороги и желтуху. Диагноз ставится клинически, с расширенным лабораторным обследованием. Начальное лечение проводят ампициллином плюс гентамицин или цефотаксим, как можно с более быстрым переходом на антибиотики с учетом чувствительности возбудителя. Неонатальный сепсис возникает с частотой 0,5—8,0 случаев на 1000 рождений. Наиболее высокий уровень заболеваемости отмечается среди новорожденных с низкой массой тела при рождении, с угнетением функции дыхания при рождении и при наличии перинатальных факторов риска со стороны матери.
Риск выше у младенцев мужского пола и новорожденных с врожденными аномалиями развития. Акушерские осложнения, например преждевременный разрыв плодных оболочек, произошедший за 18 часов и ранее до рождения ребенка, кровотечения у матери, токсинемия, стремительные роды или инфекционные заболевания у матери могут предрасполагать к развитию сепсиса у новорожденного. Этиология Ранний сепсис обычно является результатом инфицирования новорожденного во время родов. В более чем 50% случаев раннего сепсиса клинические проявления развиваются в течение 6 часов после рождения, а в течение 72 часов — у большинства пациентов. При позднем сепсисе новорожденных заражение часто происходит из окружающей среды. Стрептококки группы В и грамот-рицательные кишечные микроорганизмы вызывают 70% раннего сепсиса.
При посевах из влагалища и прямой кишки у женщин ко времени родов у 30% можно выявить колонизацию СГВ. По меньшей мере 35% их детей также будут колонизированы.
Сепсис новорождённых протекает молниеносно примерно в 15% случаев, среди хирургических.
Массивность колонизации определяет степень риска инвазии микроорганизма, которая в 40 раз выше при массивной колонизации. Хотя лишь у 1 из 100 новорожденных, колонизированных СГВ,развивается инвазивное заболевание, у более чем 50% из них развивается заболевание в первые 6 часов жизни. Нетипируемые штаммы Haemophilus influenzae все чаще являются возбудителями сепсиса у новорожденных, особенно недоношенных.
Другие грамотрицательные кишечные палочки и грам-положител ьные микроорганизмы—Listeria monocytogenes, энтерококки, стрептококки группы D, альфа-гемолитические стрептококки и стафилококки вызывают большую часть остальных случаев. Также выделяют Streptococcus pneumoniae Н.
Influenzae типа b и реже Neisseria meningitidis. Бессимптомная гонорея отмечается в 5—10% беременностей, поэтому N. Gonorrhoeae также может являться возбудителем неонатального сепсиса.
Стафилококки вызывают 30—50% позднего неонатального сепсиса, наиболее часто в связи с использованием внутри-сосудистых устройств. Выделение Enterobactercloacae £ Sakazakii из крови или ликвора предполагает загрязнение пищи. При вспышках внутри-больничных пневмоний или сепсиса, вызванных Pseudomonas aeruginosa, предполагают контаминацию оборудования для ИВЛ. Роль анаэробов остается неясной, хотя летальные исходы были связаны с анаэробной бактериемией. Анаэробы могут вызывать часть случаев сепсиса с отрицательными результатами посева крови, но наличием характерных для сепсиса изменений при аутопсии. Candida sp становятся все более значимыми причинами возникновения позднего сепсиса, развивающегося у 12—13% младенцев с очень низкой массой тела при рождении. Некоторые вирусные инфекции могут проявляться как ранний или поздний неонатальный сепсис.
Патофизиология Самым важным фактором риска в развитии позднего сепсиса является длительное использование внутрисосудис-тых катетеров. Другие причины сепсиса у новорожденных включают сопутствующие заболевания, антибиотикотерапию, длительную госпитализацию и контаминированное оборудование или растворы для внутривенного введения или приема внутрь. Заражение грамполо-жительными микроорганизмами может происходить из окружающей среды. Грамотрицательные кишечные бактерии, какправило, являются собственной флорой пациента, которая могла измениться под воздействием предшествующей антибактериальной терапии или быть заселена резистентными организмами через руки персонала или загрязненное оборудование.
Поэтому ситуации, в которых увеличивается риск контаминации этими микроорганизмами, приводят к повышению заболеваемости внут-рибольничными инфекциями. Факторами риска для развития сепсиса у новорожденных, вызванного Candida sp, являются длительное использование центральных венозных катетеров, парентеральное питание, предшествующее использование антибиотиков, некротический язвенный энтероколит и предшествующие операции.
Гематогенная и трансплацентарная диссеминация инфекции матери происходит при передаче некоторых вирусных, протозой-ных и тре-понемных возбудителей. Небольшое число микроорганизмов могут передаваться плоду трансплацентарно, однако в большинстве случаев заражение происходит внутриутробно восходящим путем или интранатально при прохождении через родовые пути, колонизированные возбудителем.
Хотя интенсивность колонизации матери напрямую связана с риском развития инвазивных заболеваний новорожденных, много матерей с низкой плотностью колонизации рожают младенцев с высокой плотностью колонизации, которые в связи с этим находятся в группе риска. Амниотическая жидкость, содержащая меконий или первородную смазку, способствует росту СГВ и Е. Таким образом, несколько бактерий во влагалище способны быстро размножаться при длительном безводном промежутке, что возможно объясняет этот парадокс. Микроорганизмы обычно попадают в кровоток плода при аспирации или заглатывании контаминированной амниотической жидкости, что приводит к бактериемии.
Восходящий путь инфицирования помогает объяснить такие феномены, как высокая частота преждевременного разрыва плодных оболочек при неонатальных инфекциях, значение воспаления плодных оболочек, повышенный риск инфицирования у близнеца, находящегося ближе к родовому каналу, и бактериологические характеристики неонатального сепсиса, которые отражают флору свода влагалища матери. Первичный очаг воспаления может локализоваться в придаточных пазухах носа, среднем ухе, легких, желудочно-кишечном тракте и может распространяться в мозговые оболочки, почки, кости, суставы, брюшину и кожу. Пневмония является наиболее распространенной инвазивной бактериальной инфекцией после первичного сепсиса.
Ранние проявления часто неспецифичные и стертые и не различаются в зависимости от этиологии. Особенно часто отмечаются снижение спонтанной активности, энергичности сосания, апноэ, брадикардия, нестабильность температуры. Лихорадка отмечается только у 10—50%, однако если сохраняется обычно свидетельствует об инфекционном заболевании. Другие проявления включают дыхательную недостаточность, неврологические нарушения, желтуху, рвоту, диарею и увеличение живота. О наличии анаэробной инфекции зачастую свидетельствует неприятный гнилостный запах амниотической жидкости при рождении. Специфические признаки поражения конкретного органа могут указать первичный или метастатический очаг. У большинства новорожденных с ранним сепсисом, вызванным СГВ, заболевание проявляется дыхательной недостаточностью, которую сложно отличить от болезни гиалиновых мембран.
Наименование: Корпус автосцепки СА-3. Чертеж колесной пары ру-1. Тип, серия, чертеж: 106.01.001-2, 106.01.001-2-01.
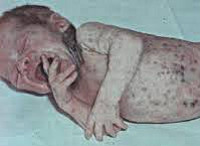
Покраснение кожи, отделяемое или кровотечение из пупочной ранки в отсутствие геморрагического диатеза предполагают омфалит. Кома, судороги, опистотонус или выбухание родничка предполагают менингит или абсцесс мозга. Снижение спонтанных движений конечностью и ее отек, эритема и местное повышение температуры или болезненность в области сустава указывают на остеомиелит или гнойный артрит. Необъяснимое вздутие живота может указывать на перитонит или некротический язвенный энтероколит. Везикулы на коже, язвы в полости рта и гепатоспле-номегалия особенно при синдроме дис-семинированного внутрисосудистого свертывания крови могут свидетельствовать о генерализованных формах герпес-вирусной инфекцииванием мазка крови.
Нормальное число лейкоцитов у новорожденных колеблется, но значения менее 4000 в мкл или более 25 000 в мкл являются отклонением от нормы. Определение абсолютного количества лейкоцитов недостаточно чувствительно для того, чтобы судить о наличии сепсиса, но соотношение юных форм и общего числа нейтрофильных лейкоцитов менее 0,2 имеет выраженное негативное прогностическое значение. Стремительное снижение абсолютного числа эо-зинофиловиморфологическиеизменения нейтрофилов например, токсическая зернистость нейтрофилов, тельца Деле и вакуолизация цитоплазмы в крови без добавления цитрата или этилендиамино-тетраацетиловой кислоты предполагают сепсис. Лаунчер робокрафт. Количество тромбоцитов может снизиться за несколько часов или дней до клинического начала заболевания, однако чаще остается повышенным в течение дня или около того после появления у новорожденного клинических проявлений.
Это снижение иногда сопровождается изменениями других показателей коагу-лограммы, характерными для ДВС-синд-рома например, увеличение продуктов деградации фибрина, снижение фибриногена, удлинение международного нормализованного отношения. Из-за большого количества циркулирующих бактерий микроорганизмы иногда можно увидеть связанными с нейтро-фильными лейкоцитами при исследовании мазка «толстой капли» при окраске по Граму, метиленовым синим или акридином оранжевым. Любальная пункция Существует риск усиления гипоксии во время ЛП у новорожденного с уже имеющейся гипоксией. Поэтому рутинное проведение ЛП не является обязательным, если уверенность в наличии сепсиса низкая.
Однако ЛП следует провести новорожденному при подозрении на сепсис так скоро, как ребенок будет способен перенести процедуру. Респираторная поддержка проводится до и в ходе ЛП для предотвращения развития гипоксии. Так как пневмонию, вызванную СГВ, которая кли СГВ-инфекции с ранним началом могут проявляться как фульминантная пневмония. Часто отмечаются акушерские осложнения. В более чем 50% случаев СГВ-инфекции проявляются в течение 6 часов после рождения; 45% новорожденных имеют оценку по шкале Апгар менее 5. Менингит часто отсутствует.
В случаях позднего начала СГВ-инфекции менингит встречается часто. СГВ-инфекции с поздним началом, как правило, не связаны с перинатальными факторами риска и очевидной колонизацией шейки матки у матери и могут быть приобретенными после родов. Диагностика Ранняя постановка диагноза имеет важное значение и требует осведомленности о факторах риска, а также настороженности, если у новорожденного отмечаются отклонения от нормы в первые несколько недель жизни. У новорожденных при подозрении на сепсис и тех, у чьих матерей предположительно имел место хориоамнионит, как можно быстрее следует взять общий анализ крови с подсчетом лейкоцитарной формулы и числа тромбоцитов, посевы крови и мочи, выполнить люмбальную пункцию, если позволяет состояние ребенка. При наличии симптомов со стороны дыхательной системы требуется проведение рентгенографии органов грудной клетки. Диагноз подтверждается выделением возбудителя бактериологическим методом.
Другие тесты могут дать отклонения от нормы, но они неспецифичны. Для недоношенных новорожденных, которые выглядят здоровыми, однако чья мать не получила адекватного противо-стрептококкового лечения во время родов, Американская педиатрическая академия рекомендует проведение ограниченного обследования. Общий анализ крови с подсчетом лейкоцитарной формулы и исследонически проявляется в первый день жизни, можно принять за болезнь гиалиновых мембран, часто ЛП проводят рутинно новорожденным с подозрением на наличие этих заболеваний. Выделение возбудителя из крови Пупочные сосуды часто контаминируются микроорганизмами с поверхности пупочной ранки, особенно через несколько часов, поэтому посевы крови из пупочных сосудов могут быть недостоверными. Следовательно, пробы крови для посева следует брать при венепункции, предпочтительно из двух периферических вен, причем место для венепункции должно быть тщательно обработано йодсодержащей жидкостью, затем 95% спиртом и в конце — высушиванием. Кровь следует сеять как на аэробную флору, так и на анаэробных возбудителей.
Если подозревают катетеризационный сепсис новорожденных, пробы для посева должны быть получены через катетер, а также при периферической венепункции. В более чем 90% положительных результатов посева крови рост отмечается в течение 48 часов инкубации; в 50% случаев положительных результатов пробы крови содержат более 50 коло-ниеобразующих единиц /мл. Поскольку это массивная бактериемия, обычно достаточно небольшого количества крови для обнаружения микроорганизмов. Данных о результатах посевов капиллярной крови не достаточно, чтобы рекомендовать их проведение. Candida sp растет в гемокультуре и на кровяном агаре, однако, если подозревают другие грибы, следует использовать среды для культивирования грибов со средней кислотностью.
Для других видов грибов, кроме Candida, может потребоваться инкубировать посевы крови в течение 4—5 дней до получения положительного результата, а возможно, и получение отрицательного результата даже в случае очевидных признаков генерализованной инфекции. Доказательства колонизации могут быть полезны до получения результатов посевов крови. Если подозревают генерализованный кандидоз, для выявления кандидозного поражения сетчатки проводят непрямую офтальмоскопию с расширением зрачка. УЗИ почек проводят для выявления мице-томы почек. Анализ и посевы мочи. Моча должна быть получена путем катетеризации или надлобковой пункции, а не с помощью мешков для сбора мочи. Хотя диагностическое значение имеют только результаты посева мочи, обнаружение более 5 лейкоцитов в поле зрения при большом увеличении в центрифугированной моче или любого количества микроорганизмов в свежей нецентрифугированной моче, окрашенной по Граму, является предварительным свидетельством наличия инфекции мочевой системы.
Отсутствие пиурии не исключает ИМС. Другие обследования для выявления инфекции и воспаления.
Изменения при сепсисе отмечаются во многих лабораторных тестах, которые оцениваются как возможные ранние маркеры. В целом, однако, чувствительность их, как правило,остается низкой до развертывания клинической картины сепсиса у новорожденных, и их специфичность не оптимальна. Реакции встречного иммуноэлектро-фореза и латекс-агглютинации позволяют выявлять антигены в биологических жидкостях; они могут использоваться, когда предварительная антибактериальная терапия делает результаты посевов недостоверными. Они могут также обнаруживать капсульный полисаха-ридный антиген СГВ, Е. Meningitidis типа В, S.
Pneumoniae, Н. Influenzae типа Ь.
Острофазовые показатели — это белки, продуцируемые печенью под влиянием ИЛ-1 при наличии воспаления. Наиболее значимыми являются тесты для количественного определения С-реактивного белка. Концентрация 1 мг/дл дает частоту ложноположительных и ложноотрица-тельных результатов 10%. Повышение С-реактивного белка происходит в течение дня с пиком на 2—3-й день и снижается до чувствительности возбудителя и локализации очага инфекции.
Если при бактериологическом исследовании нет роста возбудителя в течение 48 часов и новорожденный чувствует себя хорошо, антибактериальную терапию прекращают. Общие поддерживающие мероприятия, включая респираторную и гемодина-мическую поддержку, сочетаются с антибактериальной терапией. Антибиотики при сепсисе у новорожденных При раннем сепсисе начальное лечение должно включать ампициллин или пенициллин G плюс амино-гликозид. Вместо аминогликозида можно назначить цефотаксим. При гнилостном запахе амниотической жидкости следует добавить противоанаэробную терапию. Антибиотики могут быть изменены, как только будет выделен возбудитель.
При поступлении из дома до этого здоровых младенцев с предполагаемым поздним сепсисом они должны также получать терапию ампициллином с гентамици-ном или ампициллином с цефотаксимом. При позднем внутрибольничном сепсисе начальное лечение должно включать ван-комицин плюс аминогликозид. Если в отделении преобладает Pseudomonas aeruginosa, цефтазидим может использоваться вместо аминогликозида. Новорожденных, ранее получивших полный 7—14-дневный курс аминогликозидов, при необходимости повторного курса антибактериальной терапии должны получать другой аминогликозид или цефа-лоспорин третьего поколения. При подозрении на инфекцию, вызванную коагулазонегативными стафилококками, или коагулазонегативные стафилококки выделены из крови или другой в норме стерильной биологической жидкости и считают, что они являются возбудителем, начальная терапия позднего сепсиса новорожденных должна включать ванкомицин.
Однако, если микроорганизм чувствителен к нафциллину, следует назначить этот препарат. Удаление предполагаемого источника инфицирования и медленно возвращается к нормальному значению, значительно позже, чем наступает клиническое выздоровление.
ИЛ-6 и другие воспалительные цитокины в настоящее время изучаются как маркеры сепсиса. Сепсис новорожденных - прогноз Летальность в 2—4 раза выше среди новорожденных с низкой массой тела при рождении, чем среди доношенных новорожденных. Общая летальность при раннем сепсисе составляет 15—40% и при позднем сепсисе — 10—20%. У септических новорожденных с грану-лоцитопенией меньше шансов выжить, особенно если их пул нейтрофилов костного мозга будет снижен до менее чем 7% от общего числа ядерных клеток. Так как эти данные могут быть недоступны, отношение числа юных и общего числа нейтрофилов в периферической крови может дать приблизительное представление о пуле нейтрофилов костного мозга. Отношение Ю:0 больше 0,80 коррелирует с истощением пула нейтрофилов костного мозга и летальным исходом; это отношение может использоваться для выявления пациентов, которым может быть показана трансфузия гранулоцитов.
Сепсис Новорожденных Ppt
Лечение сепсиса у новорожденных Так как сепсис может манифестировать неспецифическими клиническими признаками, а его последствия могут быть катастрофическими, рекомендуется быстрое назначение эмпирической антибактериальной терапии; позже проводят коррекцию терапии с учетом катетера) может быть необходимо для лечения, так как коагулазонегативные стафилококки могут быть защищены глико-каликсом. Так как рост кандид может отмечаться только через 2—3 дня, начало терапии амфотерицином В и удаление инфицированного катетера без получения положительного результата посева крови или ликвора может спасти пациенту жизнь. Другие виды лечения сепсиса у новорожденных Заменное переливание крови использовалось у пациентов в тяжелом состоянии. Целью являлось увеличить уровень циркулирующих иммуноглобулинов, уменьшить уровень циркулирующих эндотоксинов, повысить уровень гемоглобина и улучшить перфузию. Однако не были проведены контролируемые перспективные исследования для оценки результатов использования за-менного переливания крови при лечении сепсиса. Свежезамороженная плазма может помочь уменьшить дефицит термолабильных и термостабильных опсонинов, который отмечается у новорожденных с низкой массой тела при рождении, однако проведение контролируемых исследований ее применения невозможно, а также следует учитывать риск, связанный с переливанием компонентов крови. Трансфузии гранулоцитов использовались у новорожденных с сепсисом и гранулоцитопенией, однако убедительных данных об улучшении прогноза получено не было.
Сепсис Новорожденных Реферат
Рекомбинантные колониестимулирую-щие факторы гранулоцитарный колони-естимулирующий фактор и гра-нулоцитарно-макрофагальный колониес-тимулирующий фактор увеличивали число нейтрофилов и их функцию у новорожденных с предполагаемым сепсисом, но, по-видимому, необязательно являются эффективными у новорожденных с тяжелой нейтропенией; требуется дальнейшее исследование их применения. Профилактика сепсиса у новорожденных Внутривенное введение иммуноглобулина при рождении может предотвратить развитие сепсиса у определенных новорожденных из групп высокого риска с низкой массой тела при рождении, однако неэффективно при уже доказанной инфекции. Так как инвазивное заболевание, вызванное СГВ, часто манифестирует в течение первых 6 часов жизни, женщины, которые ранее уже родили ребенка с СГВ, вызванным заболеванием, должны во время родов получать антибактериальную терапию, а женщины с клинической или бессимптомной бактериурией во время беременности должны получать антибиотики в то время, когда выставлен диагноз, и во время родов.